
¿Cómo se comportan las mutaciones virales?
La diversidad de organismos que habitan la naturaleza es inmensa y a la vez alucinante.
Es sorprendente pensar que por cada metro cuadrado hay millones de microorganismos como bacterias, protozoos, amebas y virus interactuando entre ellos y a su vez, interactuando con otros organismos como hongos, insectos, mamíferos, plantas, etc. Esta convivencia sucede en un mismo entorno y establece un equilibrio ecológico a través del tiempo entre especies distintas. Sin embargo, para que se dé este equilibrio, los organismos deben interactuar positiva y negativamente entre ellos.
¿Qué es un virus?
Un virus es un agente infeccioso muy pequeño. Posee un código genético que puede ser a partir de ADN o ARN, y este solo se replica dentro de las células de otro organismo. Su método de reproducción es inyectar su material genético en una célula de su hospedador y así infectar una tras otra. Cuando éste ya se ha reproducido, el agente revienta esta célula, la cual muere, y todos los virus que crecieron dentro de ella infectan a más.
Los virus y su evolución en el tiempo
La evolución de los virus depende de distintos factores y uno clave es la variación de su genoma producto de la selección natural. Esta proviene en parte de la
En virología, la tasa de mutación es la cantidad de errores efectuados por la maquinaria de la célula -ADN o ARN polimerasa- durante la replicación del genoma viral. Mientras que el término tasa de sustitución, se emplea para referirse a la cantidad de mutaciones por nucleótido que ocurren en un individuo o población.
La diferencia principal entre ambos términos es que la tasa de mutación estima la cantidad de diversidad genética que hay en una descendencia y la tasa de sustitución estima la velocidad de evolución de un linaje o taxón en particular.
Un ejemplo que da cuenta de la alta frecuencia de mutación es la aparición de nuevas cepas o variantes virales en ciertas estaciones del año, como en la temporada otoño-invierno del virus de la
Pero lo que se sabe hasta ahora es que los virus mutan dependiendo de su composición química y del tamaño de su genoma. Por lo tanto, aquellos que poseen ADN en su material genético presentan una tasa de mutación que está entre 10-8 a 10-6 sustituciones por nucleótido por célula infectada (s/n/c) y se ha visto que esta tasa de mutación se relaciona de manera inversa con la longitud del genoma, lo que quiere decir, que a mayor longitud del genoma del virus ocurrirán menos variaciones de este en el tiempo.
Por otro lado, los virus que poseen ARN presentan una mayor tasa de mutación que se encuentra en el rango de 10-6 a 10-4 s/n/c lo que se traduce en cambiar el genoma hasta 1 millón de veces más que su hospedador (Fig. 1).
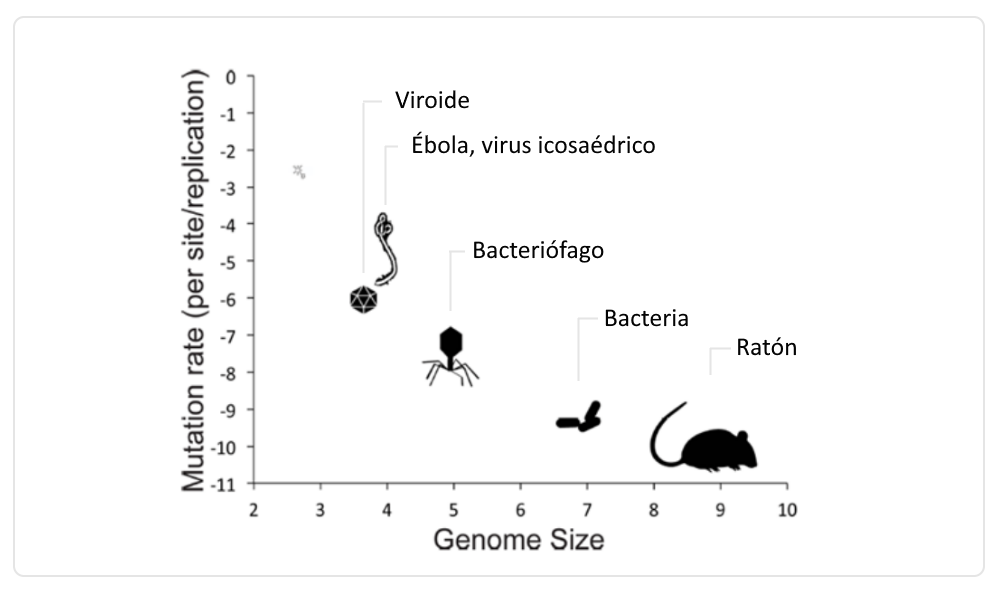
Figura 1. Variación de la tasa de mutación respecto al tamaño del genoma.
Ventajas y desventajas de las mutaciones virales
Desde el punto de vista microbiológico, la capacidad que posee el virus de relacionarse y adaptarse con su entorno es alta y se debe principalmente a las mutaciones.
En la hipótesis “Red Queen”, se postula que las interacciones ambientales competitivas virus-hospedador reflejan la capacidad que tiene el huésped (virus) para mutar con la finalidad de adaptarse al organismo/población que va a infectar.
La adaptación se da cuando un virus es capaz de evadir los mecanismos de defensa que la célula emplea para que este no la infecte, por ejemplo. Esta coevolución se da en los distintos niveles de la naturaleza, como en las bacterias, quienes poseen más de un mecanismo de defensa para evitar la infección viral con el sistema de modificación de restricción (RM) y el sistema CRISPR.
El primero se compone de enzimas que reconocen y cortan secuencias del material genético viral impidiendo que este se sintetice, mientras que el segundo es un sistema asociado a distintas enzimas CAS que corta y captura el genoma del virus para adquirir memoria y defenderse ante una segunda infección.
Sin embargo, el virus es capaz de “glicosilar” o “metilar” su material genético durante su replicación para que el sistema RM no lo reconozca. De manera similar, los virus evaden el sistema CRISPR produciendo distintas proteínas anti-CRISPR que tienen la función de bloquear la secuencia -RNA guía- que reconoce el genoma foráneo, así virus se continua su ciclo de infección.
Pero no todo es ventajoso para estas partículas nanométricas. La alta frecuencia de mutación no siempre es beneficiosa para los organismos que la padecen y en muchos casos repercute en la disminución de su descendencia.
Es por esto por lo que se debe tener claro que la mutación se producirá conforme el virus se adapte al medio ambiente que habita. Para aclarar lo anterior, en la figura 2 se observan tres genotipos virales que presentan distinta adaptación en un mismo entorno.
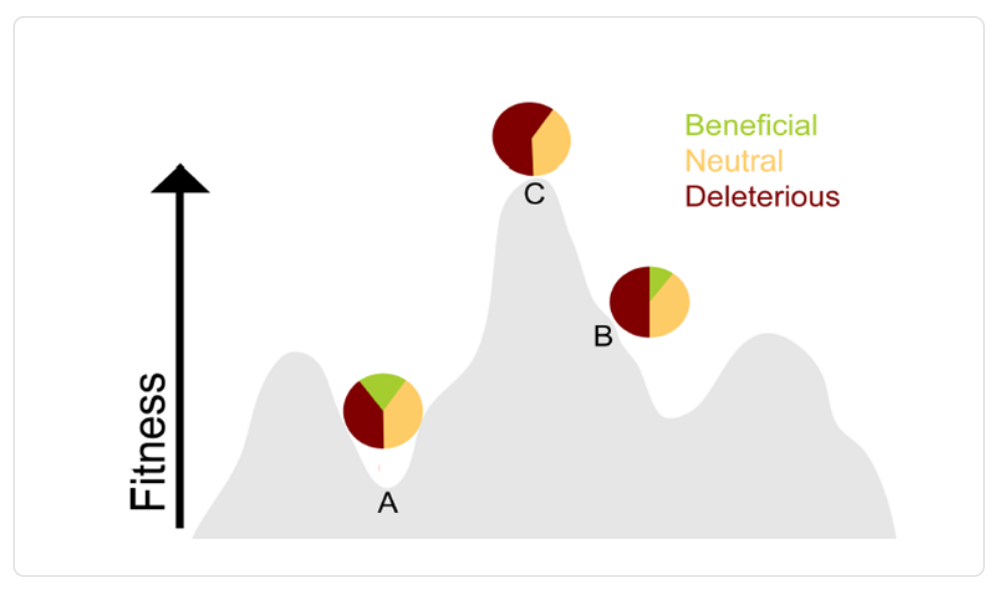
Figura 2. Adaptación de tres genotipos virales al medio ambiente.
Aquí se aprecia que el
Por otro lado, el genotipo B posee mejor adaptación al medio que el genotipo A y es por esto por lo que, si bien tiene la capacidad de seguir mutando benéficamente, la cantidad de mutaciones será menor que las del genotipo A, mientras que el genotipo C tiene la mejor adaptación en ese ambiente y no seguirá mutando de manera beneficiosa, sino que cualquier variación en su genoma repercutirá negativamente en él.
